Thèse de
Doctorat d'état es sciences physiques présentée à la Faculté des Sciences
de
l'Université de Paris
pour
obtenir le grade de Docteur es Sciences Physiques
par
G.
Chavanne
Sur
l'acide isopyromucique
soutenue le
23 juin 1904
devant la
commission d'examen :
Haller,
président
Moissan, Perrin,
examinateurs
CONCLUSION
Les recherches qui
précèdent, établissent la nature des propriétés acides de l'acide
isopyromucique et permettent de fixer la formule de constitution probable de
ce composé.
I.
L'étude de son action sur les carbonates, la mesure de sa chaleur de
neutralisation et de sa conductibilité électrique, la lenteur de son action
intervertissante sur la saccharose l'ont caractérisé comme un acide faible.
Ses propriétés acides, beaucoup moins nettes que celles de son isomère
l'acide pyromucique, sont cependant plus accentuées que celles des éthers b-cétoniques, des b-dicétones et des phénols à fonction
simple.
II.
Il doit ce caractère acide à la présence d'un groupement phénolique ou
énolique
En effet :
Les
alcools, même en présence de gaz chlorhydrique, sont sans action sur lui et
ses éthers ne peuvent être obtenus qu'en faisant agir les iodures ou les
sulfates alcooliques sur ses sels alcalins.
Le
perchlorure de phosphore donne, non un chlorure d'acide, mais un composé
analogue au phosphate triphénylique.
Les
chlorures d'acides organiques fournissent des dérivés acylés complètement
neutres qui se comportent exactement dans toutes leurs réactions comme les
éthers-sels phénoliques.
Le
groupement — C(OH) == CH — doué de propriétés acides, a d'ailleurs plutôt un
caractère phénolique qu'un caractère énolique; l'action de la phénylhydrazine
et de l'hydroxylamine n'a pas permis, en effet, de déceler la présence d'une
forme cétonique tautomère.
III.
Il possède une chaîne d'atomes de carbone, fermée par un groupement
lactonique.
Le
petit nombre d'atomes d'hydrogène contenu dans la molécule conduit, en effet,
à supposer que la chaîne d'atomes de carbone contient des liaisons multiples,
et, comme les halogènes donnent de préférence des dérivés de substitution, il
est naturel d'admettre que la chaîne est fermée.
Outre
l'atome d'oxygène, dont je viens de préciser le caractère phénolique, l'acide
isopyromucique en possède deux autres ; ils ne peuvent être rapportés ni à
une fonction aldéhydique, ni à une fonction cétonique, ainsi que cela résulte
du mode d'action de la phénylhydrazine et de l'hydroxylamine ; l'inaction des
acides nous oblige à rejeter de même les fonctions oxyde d'éthylène et
pyronique. Il ne reste donc à admettre que la fonction lactonique dont
l'existence est confirmée par les faits suivants :
1°
Décomposition de l'acide isopyromucique par l'eau, avec production
d'anhydride carbonique ;
2°
Instabilité de ce composé vis-à-vis des alcalis ;
3°
Enfin, par le fait important qu'il résulte de la lactone arabonique par la
même réaction qui l'a fournie à partir de l'acide mucique, ce qui nous
conduit à considérer cette oxylactone ou un de ses isomères stéréochimiques
comme un terme intermédiaire de sa formation.
Nous
sommes conduit, pour expliquer celle-ci et fixer du même coup sa formule de
constitution, à la suite des schémas suivants :
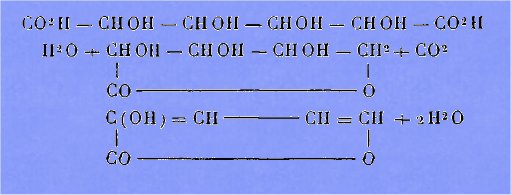
Cette formule
correspond bien aux faits :
1°
Elle rend compte des propriétés phénoliques
2°
Elle nous explique la production de dérivés pyrroliques dans la distillation
sèche de l’isopyromucate d'ammonium :
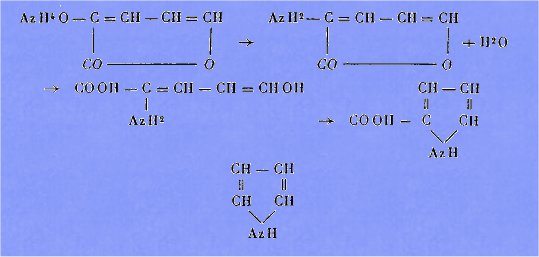
3°
Elle rend compte de la substitution du brome et du mécanisme ultérieur de
l'action de cet halogène en présence de l'eau :
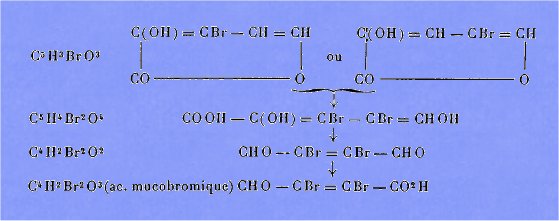
Remarque.— L'impossibilité d'obtenir avec le brome des produits
d'addition bromes nous a conduit à rejeter la formule
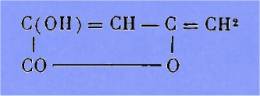
à laquelle nous aurions pu être
amené par une légère variante de la discussion.
L'apparition
constante du dérivé mucobromique nous a de même imposé la position en a de l'oxhydrile énolique qu'on aurait pu également supposer en b.
4° Enfin,
elle est encore d'accord avec cette observation que l'acide isopyromucique
paraît se former à partir des acides bibasiques des sucres en C6 indépendamment
de leur configuration, comme à partir de la lactone arabonique en C5. Si cette
remarque pouvait être généralisée, il en résulterait une nouvelle
différenciation des pentoses et des hexoses, proche parente d'ailleurs de celle
qu'on a coutume de tirer de la production du furfurol. La continuation de mes
recherches me permettra sans doute d'élucider cette importante question.
Mots clefs : action /
phénolique / propriété / isopyromucique / formule / fonction / éther / énolique / cétonique /
brome / recherche / réaction / phénylhydrazine / lactone / isomère / hydroxylamine / halogène /
constitution / chlorure / arabonique / acide / triphénylique / sucre / stéréochimique /
saccharose / pyrrolique / pyronique / pyromucique / phosphore / phosphate / phénol /
perchlorure / pentose / oxylactone / oxhydrile / organique / mucobromique / mucique /
molécule / mécanisme / isopyromucate / iodure / hexose / furfurol / chavanne / haller